
Auteur : Didier Tranchier (Ph.D)
🔍 Artificial Intelligence: A New Pharmaceutical Prescription Model – English version
L’intelligence artificielle (IA), plus précisément les Grands modèles de langage (LLM), s’est imposée en quelques années comme l’une des technologies les plus structurantes de notre époque. Si son impact sur l’ensemble des secteurs économiques est déjà largement documenté, son influence sur les pratiques médicales, et plus spécifiquement sur le modèle de prescription pharmaceutique, demeure encore insuffisamment analysée. C’est précisément l’objet de cet article : examiner comment l’IA est en train de faire émerger un nouveau modèle de prescription, plus puissant que le modèle traditionnel, mais qui soulève une question fondamentale de souveraineté que les laboratoires pharmaceutiques ne peuvent plus ignorer.
Pour saisir pleinement l’ampleur de cette transformation, il convient d’abord d’examiner les fragilités structurelles du modèle qu’elle vient supplanter.
-
Un modèle de prescription physique en plein déclin
Précisons d’emblée ce que nous entendons par modèle de prescription physique des produits pharmaceutiques : il s’agit de l’ensemble des actions visant à informer les médecins sur les spécialités pharmaceutiques au moyen de contacts et de supports physiques, afin d’accroître leur fréquence de prescription. Ce modèle repose sur plusieurs fonctions clés au sein des laboratoires pharmaceutiques :
- Les forces commerciales qui vont directement visiter les professionnels de santé, les hôpitaux, les officines de pharmacies
- Les affaires médicales qui assurent la diffusion des informations scientifiques et médicales auprès des professionnels de santé de manière individuelle ou collective, notamment dans les congrès, et promeuvent des projets à visée clinique ou thérapeutique, notamment de recherche
- Le marketing, qui produit des contenus et organise des campagnes à destination de l’ensemble de l’écosystème
La performance de ce modèle est remise en question de longue date. À titre d’illustration, une revue de la littérature scientifique publiée dès 2010 met en évidence l’absence d’efficacité systématique démontrée.
Par ailleurs, la restriction croissante et continue de l’accès aux médecins a dégradé l’efficacité de ce modèle tout en en alourdissant le coût. Le développement accéléré des outils numériques n’a pas inversé cette tendance : bien qu’il ait introduit de nouveaux canaux d’interaction, il n’a pas permis de restaurer l’efficacité du modèle.
Dans ce contexte, l’arrivée de l’intelligence artificielle ne fait pas que fragiliser ce modèle, elle le rend obsolète, en créant un nouveau modèle radicalement différent.
-
L’IA est déjà le principal outil de référence des médecins et des patients
Depuis le lancement de ChatGPT 3.5 le 30 novembre 2022, l’adoption de ces outils a connu une progression sans précédent, comme l’illustre la figure 1 ci-dessous :
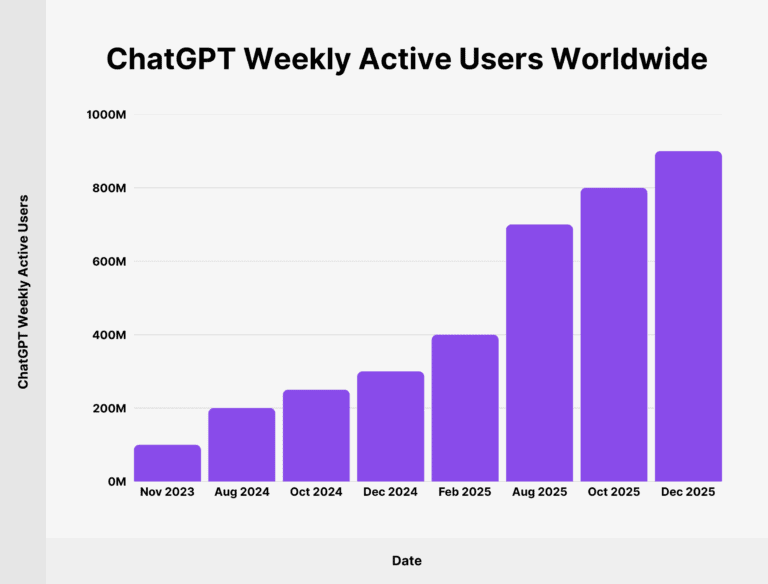
Figure 1 : Evolution dans le temps du nombre d’utilisateurs de ChatGPT, source : https://backlinko.com/chatgpt-stats
Contrairement à ce qui s’est produit avec les moteurs de recherche, l’écosystème de l’IA générative ne se réduit pas à un acteur dominant : si ChatGPT constitue l’outil le plus utilisé, une multiplicité d’autres solutions coexistent, dont plusieurs sont spécifiquement conçues pour le domaine médical.
Les données disponibles attestent d’une pénétration déjà significative de ces outils dans la pratique médicale :
- Une étude française du Healthcare Data Institute datant de 2023 montre que 41,47% des médecins en France utilisent l’IA au moins 1 fois par mois
- Une autre étude américaine publiée par l’AMA (American Medical Association) le 12 mars 2026 montre que plus de 80% des médecins américains utilisent les outils d’intelligence artificielle en 2026, à comparer avec le chiffre de 38% en 2023
- Et en ce qui concerne les patients, OpenAI déclare que sur ses 800 millions d’utilisateurs réguliers, 1 sur 4 (25%) soumet un prompt sur la santé chaque semaine
Et au-delà de l’usage, les premières études cliniques montrent que les recommandations des LLMs influencent réellement les décisions thérapeutiques : une étude publiée dans Nature Medicine en 2025 sur 50 médecins américains montre que les recommandations de GPT-4 ont conduit les médecins à modifier leurs décisions cliniques initiales, avec une amélioration mesurable de leur précision diagnostique.
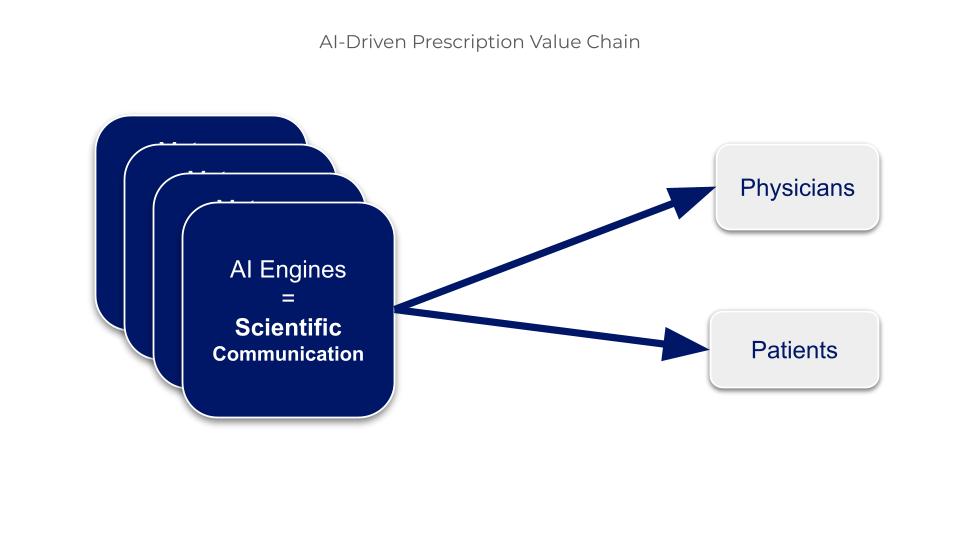
Figure 2. L’Intelligence Artificielle principal influenceur et prescripteur pour les médecins et les patients
Jusqu’à présent, on parlait beaucoup de l’influence de Dr Google, mais Dr IA est devenu le plus puissant influenceur de tout l’écosystème de la santé. Ce glissement pourrait être perçu comme une simple substitution d’interface ; il s’agit en réalité d’un changement de nature fondamentalement différent : là où Google se limite à référencer des pages web sans en évaluer la fiabilité, les outils d’IA synthétisent et hiérarchisent l’information en privilégiant la littérature scientifique validée ; pour une question médicale, Dr IA répond en médecin, pas en moteur de recherche.
-
Le pouvoir de prescription de Dr IA est directement lié aux publications scientifiques médicales avec des données longitudinales
Les outils de GEO (Generative Engine Optimization), qui servent à l’optimisation pour les moteurs génératifs, permettent d’identifier les principales sources qui contribuent à créer les réponses aux questions des utilisateurs. Il existe d’ailleurs des outils spécifiques au monde de l’industrie pharmaceutiques comme PharmaGEO, développé par l’entreprise Aikka.
Ce type d’outil permet d’identifier, pour chaque moteur d’intelligence artificielle, les principales publications scientifiques médicales qui étudient toutes les molécules et tous les médicaments.
Autrement dit, la communauté scientifique des médecins qui publie dans les journaux scientifiques alimente directement les moteurs d’intelligence artificielle et donc tous les médecins et les patients.
Mais pour produire un article scientifique médical de qualité, il faut disposer de cohortes de données en volume, structurées, homogènes, longitudinales et spécifiques à une aire thérapeutique. Et les meilleures sources de ces données sont, sans aucun doute, les applications de santé digitale qui suivent le patient tout au long de son traitement médical.
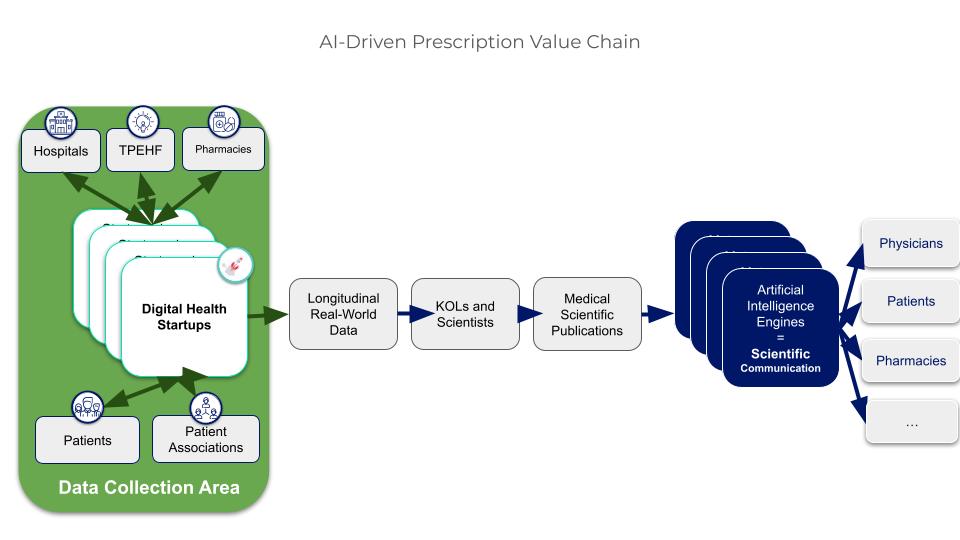
Figure 3. Les startups de santé digitale sont les meilleures sources de données en vie réelle pour les articles scientifiques
En effet, la littérature montre que la valeur des données digitales est principalement reconnue lorsque ces données sont reliées à une pathologie ou à une indication clairement définie, à des outcomes cliniques et à des décisions thérapeutiques, ce qui est typiquement le cas des solutions ciblées par aire thérapeutique plutôt que des applications généralistes de santé ou de bien‑être.
Pour accéder aux patients à l’échelle requise, ces startups doivent nécessairement être soutenues par les principaux acteurs du système de santé : les médecins, en particulier au sein des établissements hospitaliers, mais aussi les associations de patients et les officines pharmaceutiques.
Mentionnons, de même, le rôle nouveau et particulier des Tiers-Lieux d’Expérimentation, une initiative récente du gouvernement français pour permettre de créer des expérimentations au sein de l’hôpital avec des startups de santé digitale. Il y a aujourd’hui 37 TLE en France et leur avenir est encore incertain alors que leur utilité est fondamentale dans cette nouvelle création de valeur.
La valeur de ces startups, et de leurs données, est en effet directement proportionnelle à leur capacité de déploiement : plus le volume de données collectées est important, plus leur utilité scientifique et stratégique s’accroît.
Or, on assiste parfois à un foisonnement de startups sur une même spécialité ou aire thérapeutique, créant souvent de la confusion pour le choix de l’une ou l’autre de ces solutions. Nous allons donc maintenant voir que cette phase est transitoire : pour chaque aire thérapeutique prise séparément, cardiologie, diabétologie, oncologie, etc., on peut prédire qu’un petit nombre d’acteurs seulement va s’imposer. Toutefois, cette concentration ne se fera pas aussi rapidement ni aussi uniformément que dans d’autres marchés numériques : la réglementation très variable selon les pays, la résistance des institutions hospitalières à la dépendance vis-à-vis d’acteurs privés, et la fragmentation naturelle par spécialité sont autant de freins qui ralentiront le processus. C’est précisément pourquoi les laboratoires pharmaceutiques qui souhaitent prendre position n’ont pas d’intérêt à attendre et la raison pour laquelle les modèles collaboratifs ouverts, que nous examinerons en section 6, seront la condition sine qua non du succès de ces acquisitions.
Une situation paradoxale se dessine : les startups de santé digitale sont au cœur de la nouvelle chaîne de valeur de la prescription, et pourtant elles restent économiquement fragiles. Pour comprendre comment ce paradoxe pourrait se résoudre, l’histoire des ERP offre un éclairage saisissant.
-
Les startups de santé digitale sont les ERP du système de santé
La santé digitale est depuis longtemps reconnue par les grandes organisations internationales comme un levier fondamental de transformation de nos systèmes de santé : l’Assemblée mondiale de la Santé a adopté à l’unanimité une résolution sur la santé digitale, et l’OMS a défini une stratégie mondiale visant à faire des systèmes de santé des systèmes centrés sur les personnes et activés par le digital.
Il n’en demeure pas moins que ces mêmes startups peinent à trouver un modèle économique viable leur permettant de croître et de consolider leur valeur sur le marché.
En effet, aujourd’hui, en France, les principaux modèles d’affaires pour les startups de santé digitale sont :
- la vente directe aux médecins, aux hôpitaux et/ou aux patients
- le remboursement des solutions de télémédecine par la sécurité sociale
- le remboursement des thérapies digitales par la sécurité sociale
Le remboursement des solutions de télémédecine et des thérapies digitales en France, lancé après celui de l’Allemagne, semblait, à un moment, donner un cadre qui permettrait l’émergence de la santé digitale. Aujourd’hui, on s’aperçoit qu’il n’en est rien, l’obtention du remboursement est à la fois un processus long et compliqué et qu’il n’est pas la garantie d’un succès commercial.
C’est la raison pour laquelle l’apparition de ce nouveau modèle de prescription par l’intelligence artificielle peut devenir rapidement le vrai catalyseur pour développer la santé digitale.
L’analogie avec les ERP (Enterprise Resource Planning) est éclairante. Ces logiciels, déployés dans toutes les entreprises à partir de la fin des années 90, ont permis de définir pour chaque organisation les données importantes à collecter, puis de créer un tableau de bord centralisé offrant une vision globale de son fonctionnement , c’est ainsi que les entreprises ont pu piloter leur transformation.
Il est possible d’utiliser cette analogie pour mieux comprendre comment les solutions de santé digitales, en définissant les données pour chaque aire thérapeutique, puis en collectant ces données dans toutes les composantes du parcours de soin, vont permettre d’avoir une vision globale basée sur des données pertinentes et homogènes.
En définitive, si la valeur de ces données est aussi fondamentale que celle des ERP pour les entreprises, alors celui qui contrôle ces startups contrôle demain une partie du pouvoir de prescription. C’est précisément ce qui va déclencher une course à l’acquisition.
-
La raréfaction des startups de santé digitale : un effet d’aubaine pour les laboratoires pharmaceutiques
L’expérience des marchés numériques permet d’identifier une dynamique récurrente. Une première phase d’exploration voit émerger de nombreuses solutions concurrentes : les utilisateurs adoptent généralement la première solution disponible et témoignent d’une certaine réticence à en multiplier l’usage. Progressivement, une sélection s’opère : les solutions les moins performantes disparaissent tandis que celles bénéficiant du plus grand déploiement attirent de nouveaux utilisateurs, sensibles aux effets de réseau. Ce processus accélère la concentration du marché vers une structure oligopolistique, où un petit nombre d’acteurs se partagent l’essentiel du marché.
Cette situation oligopolistique place les startups dans une position de force : maîtresses d’une part de marché significative, elles sont en mesure d’imposer des conditions contractuelles favorables aux laboratoires pharmaceutiques souhaitant y accéder, ce qui contribue à accroître leur valorisation. Face à ce rapport de force, les laboratoires ont le choix entre deux stratégies pour sécuriser leurs partenariats : l’acquisition directe ou la prise de participation au capital.
Plusieurs opérations illustrent déjà cette tendance :
- Rachat de Flatiron Health en 2018 par les laboratoires Roche pour un montant de 1,9 milliards de dollars
- Partenariat et investissement dans Aetion par Sanofi en 2019
Par ailleurs, tout laboratoire acquérant l’une de ces startups se constituerait le contrôle exclusif d’une ressource rare et stratégique. À mesure que le nombre d’acteurs se réduira, l’acquisition de ces plateformes créera un véritable effet d’aubaine : les laboratoires en position de contrôler l’accès à ces données pourraient en priver leurs concurrents, constituant ainsi un avantage compétitif durable au détriment de ceux qui auront différé leur décision.
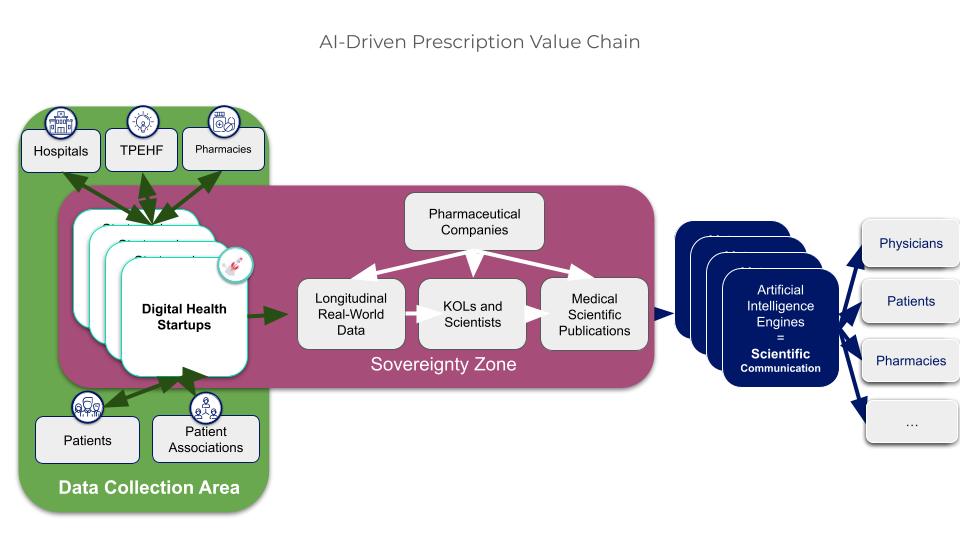 Figure 4. L’acquisition des startups de santé digitale crée un phénomène d’aubaine pour les laboratoires pharmaceutiques
Figure 4. L’acquisition des startups de santé digitale crée un phénomène d’aubaine pour les laboratoires pharmaceutiques
Cette stratégie d’acquisition n’est cependant pas sans risques : le contrôle d’une startup par un laboratoire pharmaceutique crée des tensions potentielles avec l’écosystème dont dépend précisément la valeur de cette startup.
-
L’architecture collaborative ouverte : condition de pérennité des acquisitions
En effet, l’intérêt des laboratoires pharmaceutiques peut ne pas être totalement aligné avec toutes les composantes de l’écosystème qui alimentent la valeur de la startup et qui permettent la production de ces données de qualité.
De véritables tensions peuvent apparaître entre ceux qui contrôlent la startup et l’écosystème qui l’entoure, ce qui peut aboutir à un conflit et à un rejet de la startup.
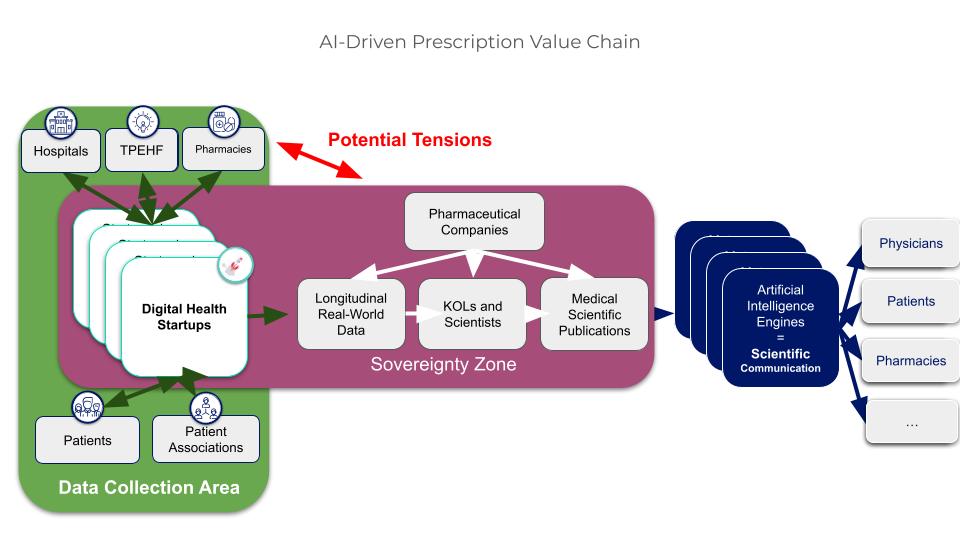
Figure 5. Illustration des tensions potentielles entre laboratoires pharmaceutique et écosystème de santé
Pour qu’une telle acquisition soit pérenne, le laboratoire pharmaceutique qui contrôle la startup ne peut pas se comporter en prédateur vis-à-vis de l’écosystème qui en constitue la valeur. Trois conditions sont indispensables : premièrement, une gouvernance multi-acteurs qui aligne les intérêts de chacun autour d’objectifs partagés ; deuxièmement, un modèle de partage de la valeur qui bénéficie à l’ensemble des contributeurs : médecins, hôpitaux, associations de patients, officines, sans lesquels les données ne peuvent pas être produites ; troisièmement, une capacité d’expérimentation concrète sur le terrain, qui valide l’utilité des solutions et génère des preuves de valeur réelles. Ces trois conditions définissent ce que l’on peut appeler une architecture collaborative ouverte.
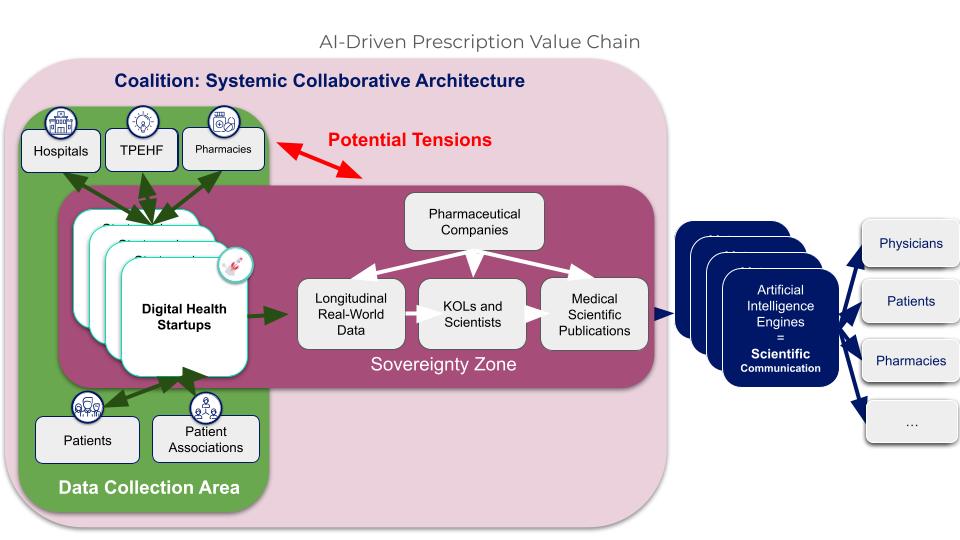
Figure 6. Il faut créer des coalitions qui alignent les intérêts des acteurs de l’écosystème santé
NextGen Coalition, co-fondée et opérée par Digital Pharma Lab depuis 2020, constitue aujourd’hui le modèle de référence de ce type d’architecture en France. En cinq ans, elle a réuni plus de 40 établissements partenaires, hôpitaux, laboratoires pharmaceutiques, startups et institutions, autour d’une gouvernance collective, avec 3,5 millions d’euros mobilisés et plus de 35 projets innovants soutenus, couvrant des parcours de soins digitaux, du télé-monitorage et des outils d’IA pour les cliniciens et 100 000 patients utilisateurs qui bénéficient déjà des solutions expérimentées dans ce cadre.
Dans le domaine officinal, Coalition IDEO, également portée par Digital Pharma Lab, applique le même principe à un écosystème différent. Elle réunit industriels de santé, groupements de pharmacies, répartiteurs et experts digitaux autour d’un objectif commun : accompagner les officines dans l’intégration du digital, alors que le métier de pharmacien se diversifie rapidement : vaccination, dépistage, accompagnement thérapeutique. Chaque année, un appel à projets co-construit avec l’ensemble des membres sur six mois de travail collectif sélectionne les solutions les plus prometteuses, garantissant que les besoins réels des officines et des patients sont au cœur de la démarche. Le premier appel à projets a permis de recevoir 42 candidatures, dont 11 ont été présentées devant la Coalition et 4 projets ont été sélectionnés et sont actuellement en cours de finalisation et de déploiement.
Ces deux exemples illustrent une leçon essentielle : la valeur d’une coalition ne se décrète pas, elle se construit patiemment, par la preuve. Ce qui rend ces modèles robustes, c’est précisément qu’ils ne sont pas contrôlés par un seul acteur : ils fonctionnent parce que chaque partie prenante y trouve un intérêt réel et mesurable. C’est ce modèle que les laboratoires pharmaceutiques qui acquièrent des startups de santé digitale devront reproduire et institutionnaliser, sous peine de détruire la valeur même qu’ils cherchent à capturer.
-
Conclusion, l’IA va créer un cercle vertueux valorisant les startups de santé digitale et des vrais systèmes collaboratifs au bénéfice de tous
L’intelligence artificielle est en train de recomposer en profondeur le modèle de prescription pharmaceutique en offrant aux médecins comme aux patients des réponses fondées sur la littérature scientifique validée. Dans cette nouvelle configuration, les startups de santé digitale qui produisent des cohortes de données en volume, structurées, homogènes, en temps réel, longitudinales et spécifiques à une aire thérapeutique permettront la production de publications scientifiques fondées sur une vision globale, quantitative et représentative du parcours thérapeutique.
Pour assurer leur souveraineté et consolider leur avantage concurrentiel, les laboratoires pharmaceutiques auront tout intérêt à acquérir ou contrôler ces startups. Mais ils devront, pour ce faire, construire de véritables architectures collaboratives ouvertes, capables d’aligner les intérêts de l’ensemble des acteurs de l’écosystème autour de cette nouvelle chaîne de valeur, condition sine qua non d’un changement systémique durable, au bénéfice de l’ensemble du secteur.
Bibliographie
Gagnon, M. A., & Lexchin, J. (2010). Information from pharmaceutical companies and the quality, quantity, and cost of physicians’ prescribing: A systematic review. PLOS Medicine, 7(10), e1000352. https://journals.plos.org/plosmedicine/article?id=10.1371/journal.pmed.1000352
Romanow, K. (2015, August 18). Crossing the threshold: More than half of physicians restrict access to sales reps. PR Newswire. https://www.prnewswire.com/news-releases/crossing-the-threshold-more-than-half-of-physicians-restrict-access-to-sales-reps-300136525.html
PR Newswire. (2016, July 14). As doctors keep closing doors on pharma reps, do digital communications provide a better solution? PR Newswire. https://www.prnewswire.com/news-releases/as-doctors-keep-closing-doors-on-pharma-reps-do-digital-communications-provide-a-better-solution-300317132.html
Healthcare Data Institute. (2023). Les Français, les professionnels de santé et l’intelligence artificielle. https://healthcaredatainstitute.com/wp-content/uploads/2024/01/etudes-hdi-day-2023_compressed_compressed-1.pdf
American Medical Association. (2026, March 12). More than 80% of physicians use AI professionally: AMA survey.
https://www.ama-assn.org/practice-management/digital-health/more-80-physicians-use-ai-professionally-ama-survey
Fierce Healthcare. (2024). 40M people use ChatGPT to answer healthcare questions, OpenAI says. https://www.fiercehealthcare.com/ai-and-machine-learning/40m-people-use-chatgpt-answer-healthcare-questions-openai-says
Semigran, H. L., Linder, J. A., Gidengil, C., & Mehrotra, A. (2017). The effect of Dr Google on doctor–patient encounters in primary care: A quantitative, observational, cross-sectional study. BMC Family Practice. https://pmc.ncbi.nlm.nih.gov/articles/PMC6169945
Staudenmayer, K. L., et al. (2025). Physician clinical decision modification and bias assessment in a randomized controlled trial of AI assistance. Communications Medicine (Nature). https://www.nature.com/articles/s43856-025-00781-2
Wikimedia Foundation. (2024). Optimisation pour les moteurs génératifs. Wikipédia. https://fr.wikipedia.org/wiki/Optimisation_pour_les_moteurs_g%C3%A9n%C3%A9ratifs
Aikka. (s.d.). PharmaGEO. https://www.aikka.ai/
Neves, A. L., et al. (2023). Digital health technology for real-world clinical outcome measurement using patient-generated data: Systematic scoping review. Journal of Medical Internet Research, 25, e46992. https://www.jmir.org/2023/1/e46992/
GNIUS – Espace Numérique de Santé. (2023). Les Tiers-Lieux d’Expérimentation en santé (TLE) – fiche acteur. https://gnius.esante.gouv.fr/fr/acteurs/fiches-acteur/tiers-lieux-dexperimentation-en-sante-tle
GNIUS – Espace Numérique de Santé. (2023). Les Tiers-Lieux d’Expérimentation en santé (TLE) – programmes nationaux. https://gnius.esante.gouv.fr/fr/programmes-nationaux/tiers-lieux-dexperimentation
Sinsky, C., et al. (2018). Digital health and health systems of the future. National Library of Medicine. https://pmc.ncbi.nlm.nih.gov/articles/PMC6203414/
Wikimedia Foundation. (2024). Thérapie numérique ou digitale. Wikipédia. https://fr.wikipedia.org/wiki/Th%C3%A9rapie_num%C3%A9rique
Wikimedia Foundation. (2024). Progiciel de gestion intégré. Wikipédia. https://fr.wikipedia.org/wiki/Progiciel_de_gestion_int%C3%A9gr%C3%A9
Digital Pharma Lab. (s.d.). NextGen Coalition. https://www.digitalpharmalab.com/en/nextgen-coalition/
Digital Pharma Lab. (s.d.). Coalition IDEO – Innovation Officine. https://www.digitalpharmalab.com/coalition-ideo-innovation-officine/
Wikimedia Foundation. (2024). Grand modèle de langage. Wikipédia. https://fr.wikipedia.org/wiki/Grand_mod%C3%A8le_de_langage
26 JUIN. 2025

05 MAI. 2025
